Ergebnis 1 bis 2 von 2
Thema: Entropieänderung
-
25.01.2016, 15:51 #1Daniel04


Entropieänderung
Guten Tag, ich hätte eine kleine Verständnisfrage zum Thema Entropie.
Es geht um folgende Aufgabe.
[csBlei]=spez. Wärmekapizität von BleiCode:Beim silvesterlichen Bleigießen werden 645 g Blei (530°C) in 0,6 l Wasser (10°C) gegossen. Welche Endtemperatur stellt sich ein? Wie groß ist die Entropieänderung? Schmelztemperatur von Blei: 327°C, spez. Schmelzwärmenge von Blei: 23,0 J/g, csBlei = 0,129 J/(g*K)
[cws]=spez. Wärmekapizität von Wasser
Aufgabe ist soweit gelöst von mir.
Nur bin ich mir noch unschlüssig wie ich die Entropieänderung berechnen soll.
Folgende Formel würde ich für die Entropieänderung des Wassers nutzen.
s=m*cws*ln(Tnach/Tvor)
Für die Entropieänderung von Blei würde ich den Vorgang in drei Teile aufteilen.
Zuerst würde ich die Entropieänderung berechnen von dem Zeitpunkt null bis vor dem Zeitpunkt, wo das Blei seinen Aggregatzustand ändert.
Also von 530°C bis 327°C.
Nun würde ich die Änderung berechnen zu dem Zeitpunkt, wo sich konkret der Aggregatzustand ändert.
Folgende Formel würde ich dazu nutzen.
s=Q/T
[Q]=Wärmemenge
Im letzten Schritt würde ich das selbe Verfahren wie im ersten Schritt nutzen. Ausgehend von 327°C bis zu der Gleichgewichtstemperatur.
Abschließend würde ich die Summe der Änderung ausrechnen.
Meine Frage ist nun, ist mein Lösungsvorschlag richtig?
-
-
26.01.2016, 12:51 #2OmegaPirat

AW: Entropieänderung
Die thermodynamische Entropie ist so definiert:
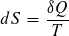
Eine Wärmemenge gibt es nicht. Wärme ist im phänomenologischen Sinne ein Energieübertrag, der ausschließlich zu einer Temperaturänderung führt und damit eine Prozessgröße, wobei in der Alltagssprache häufig Wärme mit innerer Energie verwechselt wird. Diese Definition musst du verwenden und dir dabei Gedanken machen welche Wärmen übertragen werden. Weiterhin kannst du wahrscheinlich annehmen, dass die Wärmekapazitäten von der Temperatur unabhängig sind. Dann ist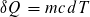 . Das in die Definition eingesetzt und integrieren liefert dann deine Formel mit dem Logarithmus.
. Das in die Definition eingesetzt und integrieren liefert dann deine Formel mit dem Logarithmus.
Deine Vorgehensweise scheint richtig zu sein.





Er "mein Herz fliegt euch zu" schon mal um 2023 (?) auf einer Konferenz gemacht - da wars aber wirklich mehr ein Herz rausreißen und werfen. Daher...
Neues von Trump, dem Unberechenbaren